Pod pojmem „perspektivní materiály“ budeme dále chápat ty materiály, které jsou již používány v praxi, ale očekává se, že v budoucnu najdou ještě mnohem větší uplatnění, než dosud. Takových materiálů je velké množství a uvedeme pouze ty, které mají návaznost na látku, vyloženou v předcházejících kapitolách.
12.1. Kovová skla
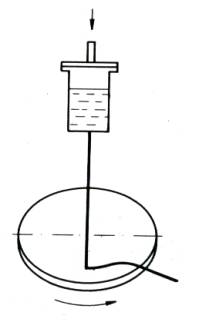
Již dříve jsme uvedli, že kapalná fáze se od fáze pevné liší mimo jiné zejména uspořádáním. Vyberme si jako příklad dvě pevné látky, sklo a kov. Pokud obě látky roztavíme, budou mí obě amorfní strukturu, typickou pro kapaliny. Po ochlazení pod teplotu tuhnutí si sklo zachová strukturu amorfní, ale kov zkrystalizuje. Příčinou tohoto odlišného chování při tuhnutí je zřejmě (kromě jiných důvodů) velikost částic, tvořících případnou krystalickou strukturu a tím pádem viskozita dané kapaliny (taveniny). V případě kovů jsou to atomy (Obr.3.3 a 3.4), v případě skel poměrně dosti velké molekuly (Obr.3.13). Proto je běžná rychlost chlazení pro roztavené sklo příliš velká (molekuly nestačí vytvořit krystalickou strukturu), zatímco pro kov je dostatečná. Z tohoto velmi názorného (a tím asi nepříliš dokonalého) kvalitativního rozboru docházíme k závěru, že chceme – li vyrobit amorfní kov, musíme ho ochlazovat velmi rychle (aby atomy nestačily „naskákat“ do mřížových bodů krystalové struktury). Výpočty a experimenty ukazují, že rychlost ochlazování by měla být řádu 105 K.s-1 (tedy ~ 100 K./ m s), což je rychlost skutečně vysoká, které u objemových předmětů nelze nikdy z pochopitelných důvodů dosáhnout (brání tomu tepelná vodivost kovů). Lze toho však dosáhnout v případě tenkých pásků, drátků a prášku. V praktickém provedení vyrábíme například pásky tak, že proud tekutého kovu lijeme mezi dva měděné a dobře vyleštěné, kapalným dusíkem chlazené válce, otáčející se proti sobě a „lisující“ a zároveň chladící tenký proud kovu. Různé obměny této metody jsou uvedeny na Obr. 12.1 – 12.4.
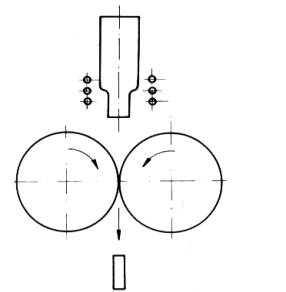
Obr.12.1. Výroba kovových skel litím mezi Obr.12.2. Výroba kovových skel litím
dva chlazené válce. na chlazený rotující kotouč.
Jak plyne z tohoto obrázku, není tato technologie nijak náročná a proto lze v současné době vyrábět již poměrně značné množství kovových skel ve tvaru drátků či pásků.
Obr.12.3. Výroba kovových
skel litím na jeden chlazený kovový buben.

Obr.13.4. Výroba kovových
skel z taveniny.
Vlastnosti kovových skel.
Amorfní struktura kovových skel vylučuje přítomnost dislokací, které jsou „produktem“ krystalického stavu a proto nedojde ani k plastické deformaci skluzem dislokací. Z toho důvodu mají kovová skla vysokou tvrdost (~ 1000 HV) a mez pevnosti řádu 2000 – 3000 MPa. Mají i zajímavé vlastnosti magnetické, které je předurčují k použití v elektrotechnickém průmyslu. Pozoruhodná je i jejich korozivzdornost, mnohem lepší, než mají nejlepší nerezové oceli (důvodem je opět nepřítomnost dislokací - dislokace totiž končí a začínají na povrchu krystalu a tam jsou reprezentovány atomem s volnou vazbou z hrany dislokace, který se ochotně naváže např. na atom kyslíku). Přestože lze kovová skla vyrobit pouze jako drátky, pásky, nebo prášek, nacházejí stále větší upotřebení v technické praxi (kvalitní výztuha pneumatik, kompozitní zpevňující vlákna ve vysokotlakých trubkách a dokonce i jako armatura ve speciálním betonu.
12.2. Uhlík.
Uhlík byl znám člověku již v pravěku jako dřevěné uhlí a saze, ale zjištění, že se jedná o prvek, bylo potvrzeno mnohem později, až v 18. století. V té době byly též určeny vztahy mezi uhlíkem, uhličitany, oxidem uhličitým, diamantem a grafitem.
Uhlík se vyskytuje jednak jako volný prvek (grafit, saze, uhlí, diamant) a jednak ve sloučeninách, uhličitanech (zejména s Ca a Mg ). Odhady celkového výskytu uhlíku v litosféře jej s jeho 180 ppm kladou na 17. místo (za Ba, Sr, S aj., ale před Zr, V, Cl, Cr. aj.).
V současné době dochází k bouřlivému rozvoji fyziky a chemie uhlíku, jehož tradiční použití jako paliva je rozšiřováno na využití při výrobě umělých diamantů, akustických i chemických senzorů, polovodičů, supravodičů, magnetů nového typu, atd. Kromě jeho tradičních modifikací (saze, grafit, diamant) byly objeveny nové modifikace (vlákna, fulerény, fulerity, fuleridy a karbyny).
12.2.1.
Krystalové modifikace uhlíku:
Diamant vytváří stejně jako Ge a Si kubickou mřížku (Obr.12.5.), kterou nazýváme v tomto případě „diamantovou“. Kromě této struktury vytváří uhlík i tzv. „diamantupodobné“ struktury (vrstvy sklovitého uhlíku).

Obr.12. 5. Diamantová mřížka.
Důkaz, že diamant je modifikací čistého uhlíku, podal již v 18. století významný francouzský chemik Antoine Lavoisier tak, že diamant spálil (za vysokých teplot). Fyzikovi P.W. Bridgmanovi se podařilo převést za vysokého tlaku a při teplotě 3000 0C diamant na grafit. Opačná cesta, kopírující svým způsobem vznik diamantů v přírodě, tj. přeměna uhlíku na diamant se podařila vyřešit až ve druhé polovině minulého století a od 60. let toho století se diamanty vyrábějí synteticky v několika zemích světa, včetně bývalého Československa (Pramet Šumperk). Syntetické diamanty se vyrábějí za tlaků 5 – 10 GPa a teplot 1500 0C – 2000 0C z grafitu. Při této výrobě je nutná přítomnost kovových katalyzátorů (Fe, Co, Ni, Cu).Fázový diagram uhlíku a jeho modifikací je uveden na Obr.12.6.
Diamant je nejtvrdší látka v přírodě, končí jím stupnice tvrdosti. Kromě klenotnictví, kde se používají zejména přírodní diamanty se velké množství diamantů horší kvality spotřebuje při výrobě řezných, brusných a obráběcích nástrojů, při výrobě korunek vrtných souprav, apod.
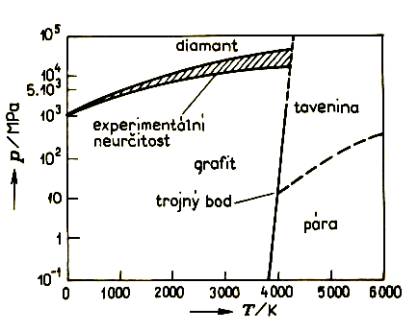
Obr.12.6. Fázový diagram uhlíku.
Struktura grafitu je znázorněna na Obr.12.7. Jedná se o typickou hexagonální mřížku.
Grafit se používá zejména jako tuhé mazivo, při výrobě tužek, apod.

Obr.12.7. Krystalová mřížka grafitu
Fulerény jsou
velké molekuly, tvořené pravidelnými mnohostěny ve tvaru koule nebo elipsoidu.
Nejstabilnější z těchto molekul, fulerén C60 (Obr. 12.8) vytváří komolý dvacetistěn, tzv.
s-ikosaedr (12 pravidelných pětiúhelníků a 20 pravidelných šestiúhelníků, takže
tvoří 32-stěn, tvarově shodných s kopacím míčem). Existují i další
uzavřené uhlíkové molekuly, např. C40, C50, C70,
a C78. Vrstvením takových molekul v pořadí ABCABC …. dostaneme
f.c.c. nadstrukturu. Látky tohoto druhu nazýváme fulerity.
Do dutin uzavřených molekul lze zabudovat další atomy (např. K, Rb aj.,) a vzniknou tzv fuleridy. Předpokládá se (a v tomto směru se koná intenzívní výzkum), že jak fulerity, tak i fuleridy mohou být supravodivé za vysokých teplot (tj. vést elektrický proud beze ztrát např. za pokojové teploty). Z molekul C60 lze vyrábět i fulerénové polymery.

Obr.12.8. Molekula fulerénu C60.
Použití fulerénů: z fulerénů lze vyrábět vysokopevnostní vlákna, maziva, molekulární membrány, akustické a chemické senzory, vodíkové zásobníky, polovodiče, supravodiče, baterie s vysokou kapacitou, katalyzátory, etická farmaceutika, aj.
Technologie výroby fulerénů: tradiční metodou výroby fulerénů je metoda, využívající vysokoteplotního uhlíkového plazmatu (získaného pomocí laseru, nebo pomocí oblouku), chlazeného proudícím heliem. V odborné literatuře jsou uvedeny další metody výroby fulerénů a protože se jedná o velmi mladé odvětví vědy, nebylo jak co do jejich použití, tak i co do způsobu jejich výroby řečeno ještě poslední slovo.
Uhlíková vlákna: uhlíková vlákna byla původně vyvinuta v 60. letech 20. století za účelem zpevňování polymerů (vznik kompozitů). Mají velmi nízkou hustotu, vysokou pevnost, vysoký modul pružnosti, snášejí vysoké teploty, jsou antikorózní a chemicky odolná. Využití mají zejména v letecké a kosmické technologii a při výrobě sportovního náčiní.
12.3. Titan.
Titan byl objeven jako chemický prvek v roce 1791 chemikem – amatérem Williamem Gregorem, farářem z Cornwallu. Německý chemik M.H. Claproth jej pojmenoval čtyři roky poté po Titánech, dětech Nebe a Země, odsouzených k životu ve skrytých ohních Země.
Titan náleží mezi hojně rozšířené prvky v zemské kůře (po hliníku a železe je to zde třetí nejrozšířenější kov). Přesto tvoří poměrně málo vydatná ložiska (ilmenit, rutil) a je v litosféře rozptýlen.
Pouhé nahlédnutí do fyzikálních tabulek nám podá první informace o vynikajících mechanických vlastnostech titanu. V Tab.12.1. uvádíme tři z těchto vlastností (hustotu r, modul pružnosti v tahu E, mez pevnosti sk a tvrdost podle Brinella HB) pro hliník, titan a železo (tři nejrozšířenější kovy a významné konstrukční materiály ve strojírenství, stavebnictví, letecké technice apod.).
Tab.12.1.
|
Prvek |
r (kg.m-3) |
E.10-10
(Pa) |
sk .10-7 Pa |
HB |
|
Al |
2700 |
7,07 |
7 |
20 |
|
Ti |
4510 |
11,6 |
30 |
155 |
|
Fe |
7874 |
21,2 |
20 |
50 |
Na základě porovnání hodnot, uvedených v této tabulce docházíme k závěru, že titan má výjimečně dobré mechanické vlastnosti. Je téměř tak lehký jako hliník a svojí pevností a tvrdostí převyšuje ocel. K dalším jeho vynikajícím vlastnostem patří vysoká korozivzdornost a skutečnost, že je velmi dobře snášen tkání lidského těla.
Z výčtu zde uvedených vlastností titanu plyne i oblast jeho použití:
- V lékařství jako náhrada lidských kostí, kloubů a zubů.
- V chemickém průmyslu díky jeho antikorozním vlastnostem na různá zařízení chemického průmyslu, přístroje, potrubí, atd.
- V kosmické a letecké technice.
- Ostatní využití, např. ve šperkařství, hodinářství, při výrobě jízdních kol, součástek automobilů, atd.
Velmi zajímavé vlastnosti má i slitina 50wt% Ni+50wt%Ti, zvaná nitinol, jedna z tzv. Onsagerových slitin. Tato slitina je významná svou vlastností, tzv. tvarovou pamětí, které lze využít opět v medicíně, strojírenství a kosmické technice. Ze stručného výčtu výjimečných vlastností titanu plyne, že je vážným kandidátem, po němž by mohla být nazvána další epocha vývoje lidstva – doba titanová.
12.4. Superplasticita.
V kapitole 6 jsme uvedli, že po překročení meze pružnosti se většina materiálů deformuje plasticky, tj. dojde k nevratné změně tvaru (např. k prodloužení vzorku). Plastická deformace je závislá na několika faktorech (např. na teplotě), ale zpravidla ani při vysokých teplotách nedosahuje relativní prodloužení vyšší hodnoty, než je 10% (neboť dříve dojde k lomu).
Přesto je znám jev, zvaný superplasticita, vyznačující se tím, že relativní prodloužení dosahuje hodnot několik set procent (jinými slovy, vzorek délky l se protáhne na několikanásobek), aniž dojde k jeho přetržení. Aby bylo možno daný kov či slitinu deformovat superplasticky, je třeba splnit dvě základní podmínky:
- Materiál musí mít velmi jemné zrno. Dosáhneme toho protlačováním materiálu (Obr.5.7.c,d).
- Proces deformování musí probíhat v určitém teplotním intervalu, závislém na materiálu, který deformujeme (0,5 – 0,65 TM, kde TM je teplota tání materiálu v K). Rychlost deformování musí být malá.
Superplastická deformace má i svůj význam praktický. Při výrobě některých součástek, které mají složitý tvar, dochází při jejich opracování (vrtání, soustružení, frézování) k velkému odpadu materiálu. Navíc je takové opracování energeticky náročné. Proto se ukazuje jako výhodnější převést materiál do superplastické modifikace (tj. zjemnit zrno a ohřát jej na žádanou teplotu), poté ho „nalisovat“ do formy žádaného tvaru, nenáročnou tepelnou úpravou ho rekrystalizovat, aby byl tvrdší a teprve potom ho mechanicky upravit na výsledný tvar.
Tímto technologickým postupem jsou v současné době vyráběny nejen některé kovové výrobky komplikovanějšího tvaru (např. automobilové karburátory), ale i výrobky z keramik (Al2O3, ZrO2) a intermetalických sloučenin (Ni3Si).
12.5. Supravodivost.
Závislost elektrického odporu vodiče na jeho rozměrech (délce l a průřezu S), materiálu a teplotě, je dána vztahem
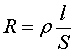 (12.1)
(12.1)
kde r je měrný odpor vodiče, závislý na jeho materiálu a teplotě.
Teplotní závislost měrného odporu většiny kovů je taková, že při teplotě velmi blízké 0K má odpor jistou malou hodnotu a s rostoucí teplotou odpor roste prakticky lineárně. V roce 1911 však zjistil holandský fyzik H. Kammerling Ones, že měrný odpor některých kovů prudce klesá na nulovou hodnotu již při teplotě vyšší, než je 0 K (tzv. kritická teplota TC). V Tab.12.2. jsou uvedeny hodnoty této teploty pro některé kovy.
Stejný badatel zjistil, že supravodivost se dá narušit působením magnetického pole o jisté prahové hodnotě (BC). Jev supravodivosti byl intenzivně zkoumán jak po experimentální, tak i po teoretické stránce. Za objasnění jevu supravodivosti byla udělena Nobelova cena za fyziku J.Bardeenovi, L.Cooperovi a J.R.Schriefferovi.
Tab.12.2.
|
Kov |
TC (K) |
Kov |
TC (K) |
Kov |
TC (K) |
|
Al |
1,18 |
In |
3,40 |
Sn |
3,72 |
|
V |
5,38 |
Ti |
0,39 |
La |
6,00 |
|
Zn |
0,875 |
U |
0,68 |
Hg |
4,15 |
|
Tl |
2,39 |
Ta |
4,48 |
W |
0,0012 |
Velký význam má jev supravodivosti po stránce technického využití. V tomto stavu má kov nulový odpor a vede tedy elektrický proud beze ztrát, takže by mohl přivést výkon celé elektrárny tenkými vodiči z libovolné vzdálenosti (ztráty výkonu při vedení elektrického proudu běžnými vodiči dosahují desítek procent). Bohužel dosud se nepodařilo získat kovový materiál (slitinu), který by měl hodnotu kritické teploty vyšší, než 25 K (např. Nb3Sn má TC = 18,3 K, Nb3Ge má TC = 23,2 K). V praxi to znamená, že supravodivý vodič musí být umístěn v ose trubice, ochlazované tekutým heliem. Vnější plášť této trubice musí být dále ochlazován tekutým dusíkem a ten samozřejmě musí být dobře izolován dalším obalem od vnějšího prostředí. Co by se ušetřilo na ztrátách ve vedení, to se spotřebuje na zkapalňování obou plynů. Proto se jevu supravodivosti v kovech a jejich slitinách používá zejména v laboratořích k získání extrémních magnetických a elektrických polí a též v kosmické technice.
V posledních desetiletích však svitla naděje na získání supravodivých materiálů jiného typu, založených na bázi keramik. Tak například v roce 1986 byla na keramickém materiálu BaxLayCuzO naměřena kritická teplota 30 K a nedlouho poté po náhradě lantanu yttriem, bariem a stronciem vzrostla postupně na 95 K a dokonce až na 125 K. Technologie přípravy takových keramických supravodičů je velmi jednoduchá, bohužel v současné době neexistuje úplná teorie vysokoteplotní supravodivosti, která by vedla bezpečně k experimentálnímu cíli – výrobě supravodiče s kritickou teplotou, alespoň o 100 K vyšší, než je teplota pokojová. Proto se experimentální výzkum zatím ubírá cestou extenzivní, tj. cestou náhodných pokusů.
Dalšími možnými materiály pro vysokoteplotní supravodiče by mohly být lineární modifikace uhlíku, tzv. karbyny.
Závěrem lze říci, že oblast výzkumu vysokoteplotních supravodičů se nachází v centru pozornosti experimentátorů i teoretiků v mnoha zemích světa, takže se zde dá očekávat v blízké budoucnosti kvalitativní pokrok, který bude mít zásadní význam pro celé lidstvo.
Seznam použité a k dalšímu studiu doporučené
literatury:
CALLISTER, W.D.: Science and Engineering. An Introduction. John Wiley & Sons, Inc.,
2000.
ASKELAND, D.R.: The Science and Engineering of Materials. Chapman & Hall, 1996.
GROOVER, M.P.: Fundamentals of Modern Manufacturing. John Wiley & Sons, Inc., 1999.
ŠESTÁK, J., STRNAD, Z., TŘÍSKA, A. a kol.: Speciální technologie a materiály. Academia Praha 1993.
POKLUDA, J., KROUPA, F., OBDRŽÁLEK, L.: Mechanické vlastnosti a struktura pevných látek. PC-DIR spol s.r.o, Brno 1994.
RABINOWICZ, E.: Friction and Wear of Materials. John Wiley & Sons, Inc., 1995
OHANIAN, H.C.: Physics.
W.W.Norton & Company 1989.
SERWAY,
R.A.: Physics. Sounders Coll.
Publishing. 1996.
BROŽ, J. a
kol.: Základy fyzikálních měření I – III.
SPN Praha, 1967.
SODOMKA,
L., FIALA, J.: Fyzika a chemie
kondenzovaných látek s aplikacemi 1 a 2. ADHESIV Liberec 2004.
PLUHAŘ, J. a kol.: Nauka o materiálech. SNTL / ALFA 1989. .